近日,中國科學院廣州生物醫(yī)藥與健康研究院許永團隊針對溴結構域家族蛋白抑制劑選擇性難題,報道了一種在急性髓系白血病(AML)治療中具有顯著療效的BRD9選擇性抑制劑Y22073(專利申請?zhí)枺?025100176011.1),為AML 精準治療提供了全新解決方案。相關成果以“Key imidazolyl groups that induce phenylalanine flipping enhance the efficacy of oral BRD9 inhibitors for AML treatment”為題發(fā)表于藥物化學領域Top期刊Acta Pharmaceutica Sinica B上。
許永團隊長期致力于創(chuàng)新藥物靶點發(fā)現、作用機制解析及創(chuàng)新藥物研究,特別是在腫瘤表觀遺傳治療領域獲得了系統(tǒng)性的研究成果(J Med Chem,?2022,65,5760;Bioorg Chem,?2024,142,106950;J Med Chem,?2024,67,6952;J Med Chem,2024,67,21577)。溴結構域蛋白9(BRD9)是哺乳動物SWI/SNF染色質重塑復合物家族中ncBAF的核心組分,該組分是目前癌癥中頻發(fā)突變的表觀遺傳調控復合物。BRD9通過特異性識別組蛋白上的乙酰化賴氨酸,招募轉錄復合物并介導下游轉錄調控與靶基因的表達。BRD9在AML等多種癌癥中發(fā)揮關鍵表觀遺傳調控功能,已成為抗腫瘤藥物研發(fā)的新興靶點。然而現有BRD9抑制劑在AML治療中始終未展現顯著的體內外療效,這嚴重制約其臨床轉化潛力。
針對溴結構域家族蛋白結構高度相似導致的抑制劑選擇性難題,團隊通過優(yōu)勢骨架化合物庫篩選、晶體結構解析以及基于結構的藥物設計,成功開發(fā)出可用于AML治療的新型BRD9選擇性溴結構域抑制劑Y22073。研究人員從基于結構活性關系(SAR)的優(yōu)化策略中發(fā)現了咪唑類化合物具有卓越的體外抗增殖活性。合作團隊通過X射線晶體結構解析(分辨率最高達1.78 ?)精準捕捉到BRD9的ZA通道存在一個獨特的“可調控開關”——Phe163翻轉開關。抑制劑中關鍵的咪唑藥效基團能夠誘導BRD9蛋白的Phe163殘基翻轉并與其形成穩(wěn)定的π-π相互作用。然而,其他溴結構域(如BRD7、BRD4、CECR2)中對應位置的殘基無法與咪唑基形成有效相互作用,直接證明了該機制的特異性。這一分子層面的突破性發(fā)現不僅顯著提升了化合物的體外活性,也使得Y22073成為首個在AML模型中展現明確疾病表型干預能力的BRD9抑制劑。研究團隊還創(chuàng)新性地采用該修飾策略對現有BRD9抑制劑進行結構改造,結果表明,經此策略修飾后的化合物在體外的活性顯著提升,進一步證實咪唑基團可通過調控獨特的Phe163開關,在提高活性方面發(fā)揮關鍵作用。Y22073表現出良好的溴結構域選擇性、代謝穩(wěn)定性、溶解性并兼具理想的藥代動力學特性,在MV4-11異種移植小鼠模型中表現出顯著的口服抗腫瘤效果,且無明顯毒性。綜合其優(yōu)異的體外活性、體內療效及成藥性特征,Y22073作為具有First-in-Class潛力的BRD9溴結構域選擇性抑制劑,為急性髓系白血病的靶向治療提供了極具臨床轉化價值的新型候選藥物。
許永課題組博士生陳智銘、助理研究員張成和沈慧為本論文的共同第一作者,許永研究員、吳錫山副研究員和張巖副研究員為通訊作者。該項目得到了國家重點研發(fā)計劃、國家自然科學基金面上項目、廣東省“一帶一路”聯(lián)合實驗室基金、中國科學院自主部署項目、中國科學院青促會項目和廣東省科技廳項目的支持。
論文鏈接??
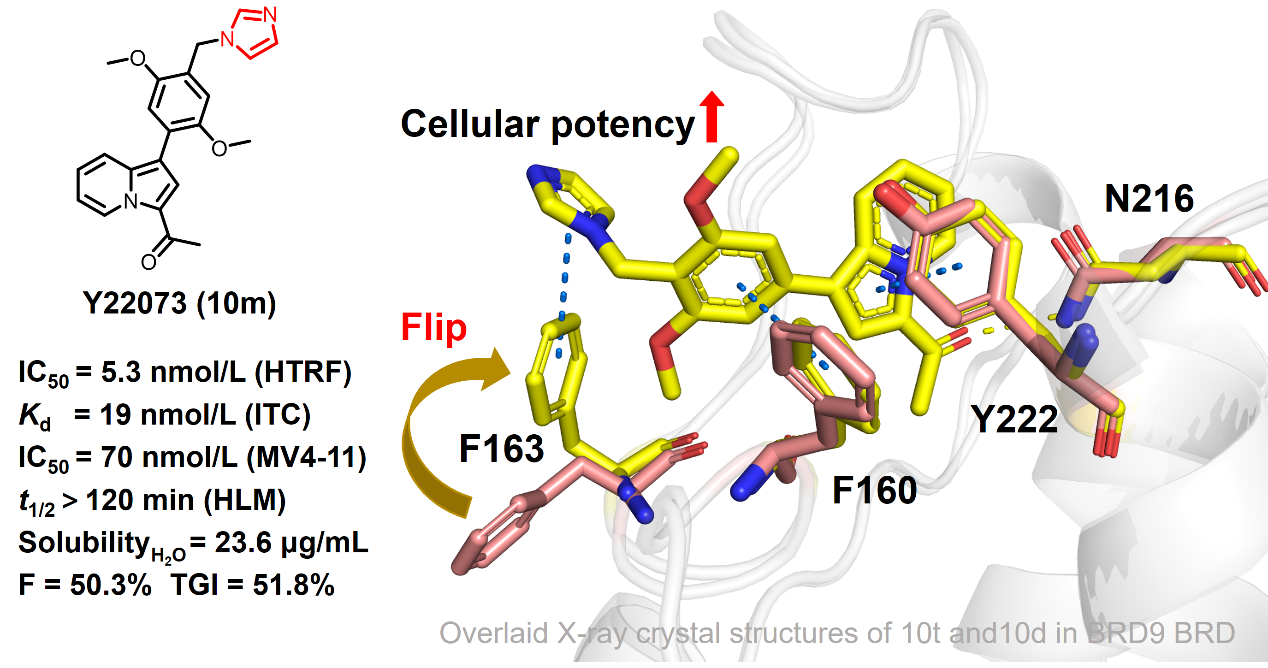
BRD9抑制劑Y22073可作為候選化合物用于AML治療
附件下載:


